FDA將在7月審查七種肽類,市場預期放寬限制助HIMS業務回溫。
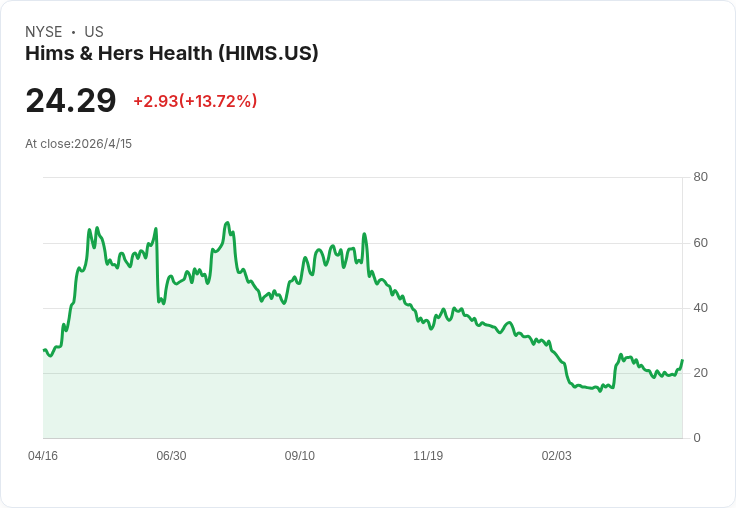
Hims & Hers(HIMS)股價在週四早盤再度大漲約6%,延續週三約13%的漲幅,投資人把焦點放在美國衛生部長羅伯特·F·肯尼迪(Robert F. Kennedy Jr.)公開表示,食品藥物管理局(FDA)將重新評估並可能放寬對某些肽類(peptides)的管制。肯尼迪在社群平臺指出,FDA會把七種肽類從「第二類」(Category 2)移出,送交藥房製劑諮詢委員會(PCAC)於7月起的會議中以科學證據逐一評估,期望恢復受監管的合法取得,並減少黑市需求。
背景與事實: - FDA目前把被認為過於危險或證據不足的藥物列為Category 2,不能在配方藥房(compounding pharmacies)生產;若移出代表將由專家依臨床、藥理與安全性資料重新審視。 - Hims & Hers去年收購了位於加州的肽類生產設施,策略上希望擴大從體重管理到肌肉修復等多項治療配方的供應能力。 - 週三與週四的股價跳動,反映市場對放寬規範、擴大合規供應的預期。 - 儘管短期利多,HIMS股價今年迄今仍下跌約23%,主要因配方化(compounded)型GLP-1減重藥的監管不確定性拖累;3月時藥廠Novo Nordisk(NVO)已撤回對該電信醫療服務商的專利侵權訴訟。 - 公司回應是,將為GLP-1使用者提供廣泛的FDA核准藥物選項,並在平臺上有限度提供配方化的semaglutide。
分析與評論: 市場把FDA即將召開的PCAC會議視為重大轉折點。若委員會接受科學證據,準許部分肽類在受監管的配方藥房內合法製造,對Hims & Hers有三大利好:一、其自有生產線可擴大合規出貨並提高毛利;二、能把客戶從風險較高的黑市或未受監管來源轉向公司平臺;三、可降低法律風險與相關訴訟的不確定性,改善投資人信心。然而,這個利多並非確定無虞——PCAC仍可能根據安全疑慮或臨床證據不足,維持限制或提出更嚴格監管條件。
駁斥替代觀點: 反對者主張FDA若放寬規範,可能造成安全事件或在品質把關上出現漏洞,增加監管與訴訟風險,對患者安全構成威脅;此外,即便允許配方化製造,保險覆蓋、市場接受度與價格競爭仍可能限制公司獲利。對此,支援放寬者與衛生部指出,送交PCAC是以科學為本的評估程式,並非任意放寬;若資料不足或風險過高,委員會可繼續維持限制,反映監管仍以安全為優先,而非單純開放市場。
結論與展望(投資人與業界應關注的重點): - 關鍵時間點為FDA/PCAC在7月起的會議與其最終結論;投資人應關注會議日程、提交的臨床與安全資料、以及委員會成員意見。 - 若評估結果偏向允許,HIMS可望在中期內受惠於合規肽類產品銷售成長;若否,短期股價可能再度承壓。 - 建議投資人與業界持續追蹤監管公告、公司在生產與合規上的準備情況、以及主要競爭對手(如NVO)在相關專利或法務動態的後續動作。 總之,FDA將肽類送交PCAC評估,為市場帶來可觀的上行預期,但安全監管與臨床證據仍是決定性變數;投資與政策制定應以等待專家審查結果與公司能否把握合規生產能力為依據。
點擊下方連結,開啟「美股K線APP」,獲得更多美股即時資訊喔!
https://www.cmoney.tw/r/56/9hlg37

 發表
發表


 我的網誌
我的網誌