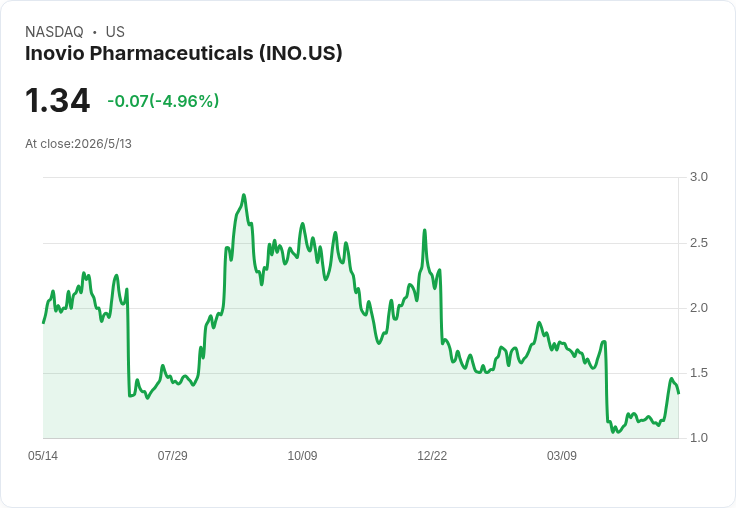
FDA中期審查無新問題,INO-3107朝10/30/2026 PDUFA邁進,現金續航延至2027年第一季。
英諾唯(Inovio)管理層在2026年第一季財報電話會中強調,公司正全力推進主力藥物INO-3107進入審核程式,目標鎖定2026年10月30日的PDUFA到期日。執行長Jacqueline Shea表示,FDA已完成標準的中期(mid-cycle)審查,未提出新重要問題,且已安排第三季的late-cycle審查,整體審查節奏正向。
背景與財務概況: 公司截至2026年第一季末現金、約當現金與短期投資合計為3,770萬美元,低於2025年12月31日的5,850萬美元。4月完成的公開增資在扣除承銷與費用後,淨募得約1,600萬美元;CFO Peter Kies指出,此舉已將公司估算的現金續航時間從先前預估的2026年第四季延長到2027年第一季。公司同時預估2026年第二季的營運淨現金燒錢約為1,800萬美元。第一季淨虧損為1,970萬美元(每股虧損0.28美元),優於市場對每股虧損0.33美元的預期;營運費用較去年同期下降13%,顯示費用管理有所改善。
臨床、監管與商業策略: 管理層表示,將在與FDA的非正式會議中聚焦加速核准(accelerated approval)資格與「有意義治療效益」的討論,並期待就確認性試驗(confirmatory trial)的設計取得回饋。公司提交給FDA的補充評估資料並未包含新臨床資料,而是進一步分析既有資料。商業面上,英諾唯計畫在美國自行執行上市活動,結合外包的合約銷售組織(CRO/CSO)支援;行銷主軸將強調INO-3107的差異性——例如不需超低溫冷鏈、也不需手術以維持給藥期間的最低殘留疾病(水準),管理階層認為這可在市場上形成區隔。就標籤與定價,執行長預期標籤與已核准產品相近,並朝罕見疾病定價思考。
風險、質疑與回應: 分析師關切焦點包括上市執行、FDA審查不確定性(例如FDA高層變動的外溢影響)與資金狀況。對此,管理層反覆強調審查似乎在正常進行,但對FDA內部運作無法評論;同時提醒投資人,現金續航的估算不含未來可能進行的資本募集。對於是否有新資料或何時會有確認性試驗明細,管理層表示將在非正式會議中尋求回饋,期望得到設計指引,但目前尚無新的長期耐久性資料讀出計畫。
分析與未來展望: 短中期關鍵觀察點包括:FDA第三季的late-cycle審查結果與非正式會議回饋、確認性試驗的最終設計、以及公司是否需進一步募資以支援商業化與試驗需求。儘管中期審查「無新重要問題」為利多訊號,投資人仍應留意現金燒錢節奏與潛在攤薄風險;若INO-3107在10/30/2026獲準,英諾唯將面臨快速轉為商業化的執行考驗。建議關注公司在未來數月就確認性試驗、FDA回饋與商業隊伍建置發出的具體進展公告。
點擊下方連結,開啟「美股K線APP」,獲得更多美股即時資訊喔!
https://www.cmoney.tw/r/56/9hlg37
 免責宣言
免責宣言
本網站所提供資訊僅供參考,並無任何推介買賣之意,投資人應自行承擔交易風險。

 發表
發表


 我的網誌
我的網誌