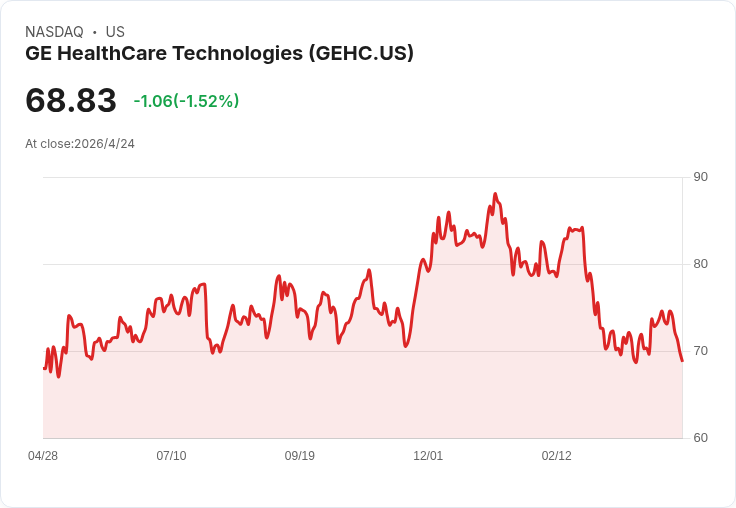
4月23日於梅約醫院首例受試者入組,GEHC推動錳基顯影劑mangaciclanol進入關鍵性試驗並獲FDA快速通道。
GE HealthCare於2026年4月23日宣佈,旗下錳(manganese)基MRI顯影劑mangaciclanol在美國梅約醫學中心完成首例病人給藥,正式啟動名為LUMINA的第2/3期臨床試驗。此試驗在FDA的Fast Track(快速通道)指定下進行,目的在加速針對重大未滿足醫療需求產品的開發與審查。
背景與試驗重點 mangaciclanol設計用於成人與兒童,主要用來協助醫師在中樞神經系統及其他部位辨識具有異常血管性的病灶。LUMINA二/三期試驗將評估其診斷效能與安全性,衡量是否能在臨床顯影品質上與目前市場主流釓基顯影劑(GBCAs)相當甚至超越。梅約醫院作為試驗場域,有助於提升早期臨床資料的信度與可見度。
為何錳基值得關注 傳統的釓基顯影劑雖然應用廣泛,但近年對於釓元素在體內長期殘留的疑慮持續成為討論焦點。相較之下,錳為人體能自我調節的天然元素,mangaciclanol採用巨環或籠狀(macrocyclic)配位結構來降低遊離金屬殘留風險。早期臨床資料顯示,其診斷能力接近市佔領先產品,若能在大規模試驗中證實安全與有效性,將有機會成為釓系顯影劑的替代方案或補充選擇,尤其在兒童與需多次造影的患者群體中具潛在優勢。
公司業務脈絡與市場意義 GE HealthCare為以影像、進階視覺化、病人照護與藥物診斷為主的醫療科技公司(分為Imaging、Advanced Visualization Solutions、Patient Care Solutions、Pharmaceutical Diagnostics等營運單位)。若mangaciclanol取得上市許可,不僅擴大公司藥物診斷產品線,也可能改變醫學影像市場的競爭格局,帶動相應影像服務與耗材需求變動。
風險、替代觀點與挑戰 儘管技術路徑與初期資料值得期待,仍存在多項不確定性:需更多大型試驗證實長期安全性與臨床優勢;監管審查過程可能耗時,且最終核准條件與標籤範圍未知;市場採用也面臨醫師使用習慣、現有供應鏈與成本考量等阻力。此外,其他廠商與研究也在開發替代顯影劑,競爭壓力不可忽視。部分投資者與分析師則認為,與快速成長且估值波動大的人工智慧類股相比,醫療器材與藥物開發雖穩健但成長節奏較慢、風險型態不同,投資取向會依風險偏好而異。
總結與展望(行動建議) LUMINA二/三期首例入組代表mangaciclanol邁入關鍵證實階段,未來幾個關鍵觀察指標包括中期與最終臨床結果、FDA審查進度、以及醫療界對安全性與影像品質的接受度。對醫療從業者與投資者而言,建議持續關注公司臨床資料發布、醫學會議成果發表與監管公告;在結果未明朗前,應平衡其長期市場潛力與臨床/監管風險,謹慎評估資產配置與決策。
點擊下方連結,開啟「美股K線APP」,獲得更多美股即時資訊喔!
https://www.cmoney.tw/r/56/9hlg37
 免責宣言
免責宣言
本網站所提供資訊僅供參考,並無任何推介買賣之意,投資人應自行承擔交易風險。

 發表
發表


 我的網誌
我的網誌